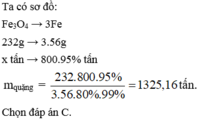Một tấn quặng manhetit chứa 81,2% Fe3O4. Khối lượng Fe có trong quặng là

Những câu hỏi liên quan
Một tấn quặng manhetit chứa 81,2% F e 3 O 4 . Khối lượng Fe có trong quặng là:
A. 858 kg
B. 885 kg
C. 588 kg
D. 724 kg
Đáp án: C
Khối lượng Fe3O4 có trong 1 tấn quặng là: 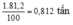
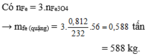
Đúng 0
Bình luận (0)
Một loại quặng sắt có chứa 81,2% F e 3 O 4 . Khối lượng Fe có trong 1 tấn quặng là:
A. 858 kg
B. 885 kg
C. 588 kg
D. 724 kg
Một loại quặng sắt manhetit chứa 90% F e 3 O 4 . Tính khối lượng của Fe có trong 1 tấn quặng trên.
Đổi 1 tấn = 1000 kg
nFe2O3 = 1000 . 90% : 160 = 5,625 (kmol)
nFe = 5,625 . 3 = 16,875 (kmol)
mFe = 16,875 . 945 (kg)
Đúng 1
Bình luận (0)
Cần bao nhiêu tấn quặng manhetit chứa 80% F e 3 O 4 để có thể luyện được 800 tấn gang có hàm lượng 95%. Lượng Fe hao hụt trong sản xuất là 1%.
A. 2351,16 tấn.
B. 3512,61 tấn.
C. 1325,16 tấn.
D. 5213,61 tấn.
Cần bao nhiêu tấn quặng manhetit chứa 80% F e 3 O 4 để có thể luyện được 800 tấn gang có hàm lượng 95%? Biết lượng Fe hao hụt trong sản xuất là 1%.
A. 5213,61 tấn.
B. 1325,16 tấn.
C. 3512,61 tấn.
D. 2351,16 tấn.
....giúp em vs ạ !... Dùng 100 tấn quặng manhetit ( Fe3O4) đẻ luyện gang ( 95% Fe ) Tính khối lượng gang thu được . Cho biết hàm lượng Fe3O4 trong quặng là 80% . Biết hiệu suất của quá trình là 93%
\(m_{Fe_3O_4}=100000.80\%=80000(kg)\\ n_{Fe_3O_4(phản ứng)}=\dfrac{80000}{232}.93\%=320,69(kmol)\\ \Rightarrow n_{Fe}=3n_{Fe_3O_4}=962,07(kmol)\\ \Rightarrow m_{Fe}=962,07.56=53875,92(kg)\\ \Rightarrow m_{gang}=\dfrac{53875,92}{95\%}=56711,49(g)\)
Đúng 1
Bình luận (0)
Một loại quặng sắt manhetit chứa 90% Fe3O4. Tính khối lượng của Fe có trong 1 tấn quặng trên.
Khối lường Fe3O4 có trong 1 tấn quặng là :
mFe3O4 = 1 x 90% = 0,9 ( tấn )
Khối lượng Fe trong Fe3O4 chiếm :
% Fe = 3 x 56 / ( 3x 56 + 4 x 16 ) = 72,41 %
Khối lượng Fe có trong 1 tấn quặng là :
mFe = 0,9 x 72,41%= 0,6517 ( tấn )
Đúng 0
Bình luận (2)
Khối lượng Fe3O4 trong 1 tấn quặng manhetit:
1: 100x90=0,9 (tấn)= 900 kg
\(\%m_{Fe}=\frac{3.M_{Fe}.100\%}{M_{Fe_3O_4}}=\frac{3.56.100}{232}\approx72,414\%\)
Khối lượng Fe:
900. 72,414%=651,726(kg)
Đúng 0
Bình luận (0)
A là quặng chứa 60% Fe2O3 , B là quặng chứa 69,6% Fe3O4 ( các tạp chất còn lại trong A , B đều không chứa Fe ) . Người ta trộn quặng A và B thu được quặng D . Từ 1 tấn quặng D có thể điều chế được tối đa 0,48 tấn Fe . Tính tỉ lệ khối lượng quặng A và B đem trộn.
Đặt mA = a (tấn); mB = b (tấn)
Giả sử a + b = 1 (tấn) (1)
\(m_{Fe_2O_3\left(A\right)}=a.60\%=0,6a\left(tấn\right)=6.10^5a\left(g\right)\)
=> \(n_{Fe_2O_3\left(A\right)}=\dfrac{6.10^5a}{160}=3750a\left(mol\right)\Rightarrow n_{Fe\left(A\right)}=7500a\left(mol\right)\)
\(m_{Fe_3O_4\left(B\right)}=b.69,6\%=0,696b\left(tấn\right)=696.10^3b\left(g\right)\)
=> \(n_{Fe_3O_4\left(B\right)}=\dfrac{696.10^3b}{232}=3000b\left(mol\right)\Rightarrow n_{Fe\left(B\right)}=9000b\left(mol\right)\)
\(n_{Fe\left(tổng\right)}=\dfrac{0,48.10^6}{56}=\dfrac{60000}{7}\left(mol\right)\)
=> \(7500a+9000b=\dfrac{60000}{7}\) (2)
(1)(2) => \(a=\dfrac{2}{7}\left(tấn\right);b=\dfrac{5}{7}\left(tấn\right)\)
=> \(\dfrac{a}{b}=\dfrac{2}{5}\)
Đúng 2
Bình luận (0)
A là quặng chứa 60% Fe2O3 , B là quặng chứa 69,6% Fe3O4 ( các tạp chất còn lại trong A , B đều không chứa Fe ) . Người ta trộn quặng A và B thu được quặng D . Từ 1 tấn quặng D có thể điều chế được tối đa 0,48 tấn Fe . Tính tỉ lệ khối lượng quặng A và B đem trộn.
Đặt mA = a (tấn); mB = b (tấn)
Giả sử a + b = 1 (tấn) (1)
\(m_{Fe_2O_3\left(A\right)}=a.60\%=0,6a\left(tấn\right)=6.10^5a\left(g\right)\)
=> \(n_{Fe_2O_3\left(A\right)}=\dfrac{6.10^5a}{160}=3750a\left(mol\right)\Rightarrow n_{Fe\left(A\right)}=7500a\left(mol\right)\)
\(m_{Fe_3O_4\left(B\right)}=b.69,6\%=0,696b\left(tấn\right)=696.10^3b\left(g\right)\)
=> \(n_{Fe_3O_4\left(B\right)}=\dfrac{696.10^3b}{232}=3000b\left(mol\right)\Rightarrow n_{Fe\left(B\right)}=9000b\left(mol\right)\)
\(n_{Fe\left(tổng\right)}=\dfrac{0,48.10^6}{56}=\dfrac{60000}{7}\left(mol\right)\)
=> \(7500a+9000b=\dfrac{60000}{7}\) (2)
(1)(2) => \(a=\dfrac{2}{7}\left(tấn\right);b=\dfrac{5}{7}\left(tấn\right)\)
=> \(\dfrac{a}{b}=\dfrac{2}{5}\)
Đúng 0
Bình luận (0)
38. Dùng quặng manhetit chứa 80% Fe3O4 để luyện thành 800 tấn gang có hàm lượng Fe là 95%. Quá trình sản xuất gang bị hao hụt 1%. Vậy đã dụng bao nhiêu tấn quặng?
A. 1325,3 B. 1311,9 C. 1380,5 D. 848,126.
39. Dùng quặng hematit chứa 90% Fe2O3 để sản xuất 1 tấn gang chứa 95% Fe. Hiệu suất quá trình là 80%. Khối lượng quặng hematit cần dùng là:
A. 1884,92kg B. 1880,2kg C. 1900,5kg D. 1905,5kg
40. Dùng 100 tấn quặng Fe3O4 để luyện gang (95% Fe, cho biết hàm lượng Fe3O4 trong quặng là 80%, hiệu...
Đọc tiếp
38. Dùng quặng manhetit chứa 80% Fe3O4 để luyện thành 800 tấn gang có hàm lượng Fe là 95%. Quá trình sản xuất gang bị hao hụt 1%. Vậy đã dụng bao nhiêu tấn quặng?
A. 1325,3 B. 1311,9 C. 1380,5 D. 848,126.
39. Dùng quặng hematit chứa 90% Fe2O3 để sản xuất 1 tấn gang chứa 95% Fe. Hiệu suất quá trình là 80%. Khối lượng quặng hematit cần dùng là:
A. 1884,92kg B. 1880,2kg C. 1900,5kg D. 1905,5kg
40. Dùng 100 tấn quặng Fe3O4 để luyện gang (95% Fe, cho biết hàm lượng Fe3O4 trong quặng là 80%, hiệu suất quá trình là 93%. Khối lượng gang thu được là:
A. 55,8 tấn B. 56,712 tấn C. 56,2 tấn D. 60,9 tấn
38. Dùng quặng manhetit chứa 80% Fe3O4 để luyện thành 800 tấn gang có hàm lượng Fe là 95%. Quá trình sản xuất gang bị hao hụt 1%. Vậy đã dụng bao nhiêu tấn quặng?
A. 1325,3 B. 1311,9 C. 1380,5 D. 848,126.
39. Dùng quặng hematit chứa 90% Fe2O3 để sản xuất 1 tấn gang chứa 95% Fe. Hiệu suất quá trình là 80%. Khối lượng quặng hematit cần dùng là:
A. 1884,92kg B. 1880,2kg C. 1900,5kg D. 1905,5kg
40. Dùng 100 tấn quặng Fe3O4 để luyện gang (95% Fe, cho biết hàm lượng Fe3O4 trong quặng là 80%, hiệu suất quá trình là 93%. Khối lượng gang thu được là:
A. 55,8 tấn B. 56,712 tấn C. 56,2 tấn D. 60,9 tấn
Đúng 0
Bình luận (0)
Câu 38:
Phản ứng xảy ra:
\(Fe_3O_4+4CO\rightarrow3Fe+4CO_2\)
Ta có:
\(m_{Fe}=80.95\%=760\left(tan\right)\)
\(\Rightarrow m_{Fe\left(tt\right)}=\frac{760}{99\%}=767,7\left(tan\right)\)
\(\Rightarrow n_{Fe}=\frac{767,7}{56}\Rightarrow n_{Fe3O4}=\frac{n_{Fe}}{3}=\frac{2559}{560}\)
\(m_{Fe3O4}=\frac{2559}{560}.\left(56.3+16.4\right)=1060,157\left(tan\right)\)
\(\Rightarrow m_{quang}=\frac{1060,157}{80\%}=1325,19625\left(tan\right)\)
Đáp án A nhé ( Nếu bạn lấy ít số sau thì sẽ ra kết quả như vậy , đây mình lần 3 số )
Câu 39:
Phản ứng xảy ra:
\(Fe_2O_3+3CO\rightarrow2Fe+3CO_2\)
\(m_{Fe}=1.95\%=0,65\left(tan\right)\)
\(\Rightarrow m_{Fe\left(lt.tao.ra\right)}=\frac{0,95}{80\%}=1,19875\left(tan\right)\)
\(\Rightarrow n_{Fe\left(lt\right)}=\frac{1,1875}{56}\)
\(\Rightarrow n_{Fe2O3}=\frac{1}{2}n_{Fe}=\frac{1,1875}{112}\)
\(m_{Fe2O3}=\frac{1,1875}{112}.\left(56.2+16.3\right)=\frac{95}{56}\left(tan\right)\)
\(\Rightarrow m_{quang}=\frac{\frac{95}{56}}{90\%}=1,885\left(tan\right)\)
P/s :Mình làm tròn số ( đáp án A nhé )
Câu 40:
\(m_{Fe3O4}=100.80\%=80\left(tan\right)\)
Trong 232 g Fe3O4 có 168 tấn Fe (do Fe chiếm 95%)
=> 80 tấn Fe3O4\(\Rightarrow\frac{168.80}{232}=57,931\left(tan\right)\)
Khối lượng Fe để luyện gang là \(57,931.93\%=53,876\left(tan\right)\)
Khối lượng gang thu được là :\(53,876.95\%=56,712\left(g\right)\)
Đúng 0
Bình luận (0)